生物陶瓷材料在牙髓再生治疗中的应用
生物陶瓷材料在牙髓再生治疗中的应用
主编〔立陶宛〕萨乌留斯·德鲁克泰尼斯(Saulius Drukteinis)
〔英〕乔赛特·卡米莱丽(Josette Camilleri)
主译 刘贺 喻健
主审 沈雅
引 言
近年来,基于生物学和微创理念的治疗技术已逐渐在临床中常规开展。这些技术充分考量了组织对于治疗的反应,改变和扩展了牙髓治疗的策略。因此,我们需要根据循证依据重新评估传统治疗方案。随着牙髓再生相关文献数量的增加和临床影响力的不断提升,该技术引起了学者们的广泛关注。有关根管内组织再生的理念可追溯到20世纪60年代,伯格·尼加德·奥斯特比(Birger Nygaard-Ostby)教授在当时阐述了“血凝块在根管治疗中的作用”。在其开展的一系列实验中,首先刺激根尖周组织,将血液引流至根管的根尖1/3,然后使用牙胶和氯仿牙胶糊剂对根管的冠部进行封闭。实验结果发现血凝块被一些组织(主要是纤维结缔组织)部分或完全替代。这些发现在当时并未引起重视,同时关于牙髓再生的实验也停滞了数十年,这期间牙髓病学领域的研究主要集中在根管的化学消毒、机械预备和充填上。临床研究发现,当年轻恒牙经外伤脱落再植入牙槽窝后,根尖周组织能够向根管内长入,这一发现推动了牙髓再生研究。相关动物实验也证实了这一发现,当根尖孔敞开的牙齿植入牙槽窝后,几周后根管中会重新形成血管网络。牙齿外伤后根管内血管网络的重新建立,即“牙髓血运重建”,对牙根的发育成熟至关重要。伊娃亚(Iwaya)等首次将牙髓再生技术应用于牙根未完全形成、伴有慢性根尖周炎和窦道形成的下颌前磨牙,他们在2001年发表的病例报道中使用了“牙髓血运重建”一词。在该病例的治疗过程中,根管冲洗后发现根管内的组织仍存在活力,因此使用氢氧化钙覆盖活性组织。术后随访时拍摄的根尖片可观察到牙根发育完成,并且牙髓电活力测试结果为阳性。班奇斯(Banchs)和特罗普(Trope)在2004年发表了一篇重要的病例报道,再次引起了学者对年轻恒牙牙髓再生治疗的关注。该病例与伊娃亚等发表的病例类似,患牙为下颌前磨牙,伴有慢性根尖周炎和窦道形成。在治疗过程中,首先使用次氯酸钠冲洗根管,然后使用三联抗生素糊剂(环丙沙星、甲硝唑和米诺环素)进行封药。根尖周炎症缓解后,通过刺激根尖周组织将血液引流进入根管。使用三氧化矿物聚合体(MTA)覆盖血凝块,并充填至釉牙骨质界水平。术后随访时拍摄的根尖片显示,根尖周病变已愈合,牙根延长、增厚,根尖闭合。学者随后发表了大量的病例报告、病例系列研究、队列研究和随机对照临床试验近期发表的系统综述和荟萃分析提供了最高等级的循证依据。
牙髓的再生和修复
多年以来,牙髓具有重要的再生和修复能力这一观点已逐渐成为共识。大约100年前,氢氧化钙就已经用于盖髓,促进牙髓组织修复。在2010年之前发表的牙髓血运重建术病例报道显示,刺激根尖周组织,将血液引流进入根管可促进牙根完全形成。这些病例报道的成功让学者对牙髓血运重建寄予厚望,认为通过血运重建可能产生牙髓组织和管状牙本质,使牙本质-牙髓复合体完全再生。由于年轻恒牙含有根尖牙乳头(一种富含间充质干细胞的结缔组织),因此有学者认为根尖牙乳头干细胞可以促进牙根发育以及牙髓生理结构与功能的恢复(图1a)。后续的研究分析了刺激根尖出血前根管中的生理盐水、从根尖引入根管中的血液以及经手臂静脉抽取的血液,探究了这些液体中是否存在间充质干细胞标记物以及浓度,结果证实从根尖引入根管的血液中存在间充质干细胞。由于根尖牙乳头中的干细胞能够分化为成牙本质细胞,因此牙髓血运重建可以实现牙髓再生这一假设似乎是合理的(图1b)。

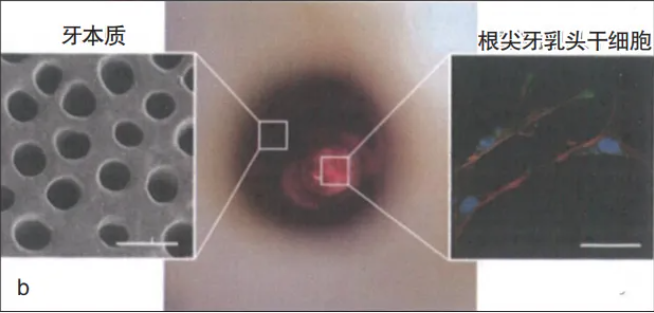
图1 a为牙髓再生治疗过程;b为牙髓再生的目标是将干细胞(根尖牙乳头干细胞;比例尺:25 mm)从根尖牙乳头中迁移至根管内,并附着在牙本质壁上(比例尺:10 μm),形成一种在结构和功能上类似于牙髓的组织
动物研究以及对人类牙齿进行的组织学分析发现,牙髓血运重建后根管中发生的是修复过程而非再生过程。在根管中形成的组织是结缔组织、牙骨质或骨组织,并不存在牙髓组织和成牙本质细胞。然而,将根尖的血液引流至根管后,形成的血凝块可以作为牙髓愈合、修复的支架和基质。不同类型的细胞从根尖周组织迁移至根管内,形成血管系统、神经组织和硬组织,这一过程与人体的创伤愈合机制类似中。近年来,学术界对于牙髓再生治疗有了更现实的认识和评估,出现了替代“牙髓血运重建”的术语“引导性牙髓修复”或“牙髓再血管化”。
临床治疗步骤
对于牙髓坏死的年轻恒牙,常规使用亲水性硅酸钙水门汀(例如MTA)来封闭未发育成熟的根尖,即“根尖封闭术”。目前在临床上可使用“牙髓再血管化”技术来替代根尖封闭术。
一般认为,在牙根发育期间越早进行牙髓再生治疗,效果可能越好。从技术角度来看,这两种治疗方式都需要患者具有较高的依从性,但与根尖封闭术相比,牙髓再血管化技术更容易进行。欧洲牙髓病学会和美国牙髓病学会关于牙髓再生治疗的指南中详细介绍了临床操作过程。尽管两份指南在临床操作细节上存在一些差异,但是口腔医师对于治疗目标以及预期的组织反应的理解和认知可能更为关键。
首次就诊时,治疗过程包括详细的临床检查、术区隔离、开髓以及对根管进行消毒。次氯酸钠是首选的消毒剂,建议使用较低的浓度(1.5%~3%)在发挥抗菌作用的同时保护干细胞和生长因子。使用生理盐水和17%乙二胺四乙酸(EDTA)冲洗根管可降低次氯酸钠对于根尖周细胞的毒性。建议不对根管进行机械预备或者进行微创预备。在根管中使用氢氧化钙糊剂封药后暂封。2~4周后复诊(图2),如果患牙炎症缓解,则进行后续治疗。在术区隔离后,使用EDTA冲洗以去除氢氧化钙并促进牙本质基质中的生长因子释放。避免使用次氯酸钠以减少对根管内微环境的影响。最后使用生理盐水冲洗根管,使用吸潮纸尖干燥根管通过刺激根尖周组织将血液引流至釉牙骨质界下方。亲水性硅酸钙水门汀可以直接覆盖血凝块,也可以将胶原海绵作为支架置于血凝块与亲水性硅酸钙水门汀之间。然后,使用粘接性修复材料封闭根管口。建议在术后6个月、12个月、18个月和24个月进行随访,此后5年中每年随访一次。
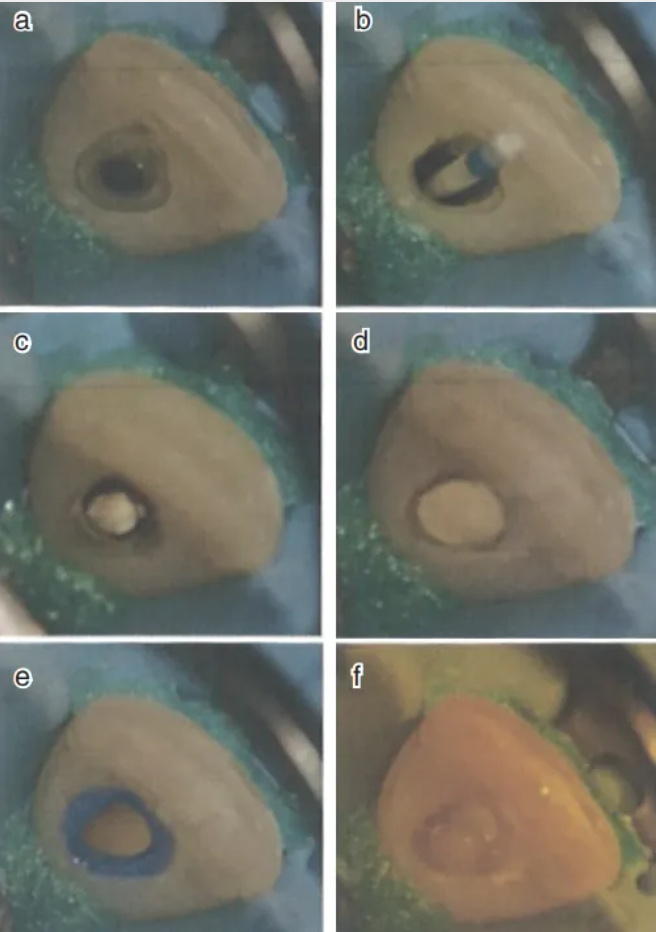

图2 上颌左侧中切牙由于外伤导致牙髓坏死,在患者第二次就诊时对患牙进行牙再血管化治疗。a为去除根管内药物,使用生理盐水和17%EDTA冲洗根管;b为干根管,刺激根尖周组织,将血波引流至根管内;c为将胶原海棉放置在血块上;d 为使用亲水性硅酸钙水门汀覆盖胶原海绵;e为对牙釉质进行选择性酸蚀;f为使用粘接剂处理窝洞;g为使用纳米复合树脂进行粘接修复
研究表明,牙髓再血管化治疗和根尖屏障术具有相似的成功率,治疗后90%以上的病例实现根尖周病变愈合,这也是美国牙髓病学会指南的首要治疗目标。
牙髓再血管化治疗与根尖屏障术相比,可能会促进牙根长度与厚度的增加。然而,研究发现这种治疗效果并不稳定。牙髓再血管化治疗后,患牙的根尖周病变可能会复发,治疗失败的原因可能是根管消毒不充分。牙髓再血管化治疗后,根管内残留的微生物并不一定会导致治疗失败,但是也可能会导致根管壁矿物质沉积减少因而不会实现牙本质壁增厚。
牙髓再血管化治疗的局限性
牙髓再血管化治疗的结果是诱导组织修复而非再生,以往观点认为这种治疗结果具有严重的局限性,然而当前观点则认为根尖周炎症的消失以及骨质愈合更重要。虽然牙髓再血管化治疗和根尖屏障术具有相似的治疗效果,但是前者可能会出现更多的并发症,例如牙冠变色、疼痛或再感染。牙冠变色可能是由牙髓再血管化治疗中使用的根管内药物、冲洗液或硅酸钙水门汀引起的,尤其是含有米诺环素的三联抗生素糊剂。这类药物可能导致牙冠严重变色,因此应尽量避免使用。
在牙根未完全形成的情况下,治疗的首要任务是避免牙颈部折裂。牙髓再血管化治疗数月后矿物沉积在牙本质壁上可以增加牙根的长度与厚度。但是将亲水性硅酸钙水门汀放置在血凝块上,在短期内会增加牙颈部折裂的风险,使用粘接树脂材料充填髓腔并封闭根管口可将折裂风险降至最低。
目前仍然缺少有关牙髓再血管化治疗的长期效果的相关数据。由于患牙预后效果不明确,因此相关正畸治疗或其他可替代的治疗方案仍存有疑问,尤其是在患者的骨骼生长阶段完成之前。综合来看,牙髓再血管化治疗的使用应慎重。
亲水性硅酸钙水门汀的应用
亲水性硅酸钙水门汀具有其他牙科材料所不具备的特殊性能,尤其是亲水性。对于大多数需要接受牙髓再血管化治疗的死髓年轻恒牙而言,MTA一直是用于覆盖血凝块的首选材料。MTA能够在潮湿的环境中固化,具有良好的生物相容性,目前市场上可替代材料较少,因此被广泛用于牙髓再血管化治疗。
MTA是对波特兰水门汀进行了改良,并添加氧化铋以增强其显影性。在固化反应过程中,MTA的主要成分硅酸三钙和硅酸二钙与水发生反应形成硅酸钙水凝胶和氢氧化钙。由于钙离子的释放与材料的抗菌作用具有相关性,因此氢氧化钙的形成有利于材料的抗菌性。波特兰水门汀是一种亲水性材料,在与水或者其他液体接触时会固化并发挥其物理性能。因此,波特兰水门汀和MTA被归类为亲水性硅酸钙水门汀。
尽管MTA已在临床上成功应用了很多年,但是仍存在一些缺点,例如MTA中含有的氧化铋会造成牙齿变色,并且MTA的固化时间长(3个小时)、操作困难且成本较高。此外,在牙髓再血管化治疗过程中,当MTA放置在血凝块上时可能会移位进入根管内(图3)。在血凝块和MTA之间使用胶原海绵作为支架材料有助于支撑MTA以防止其移位。
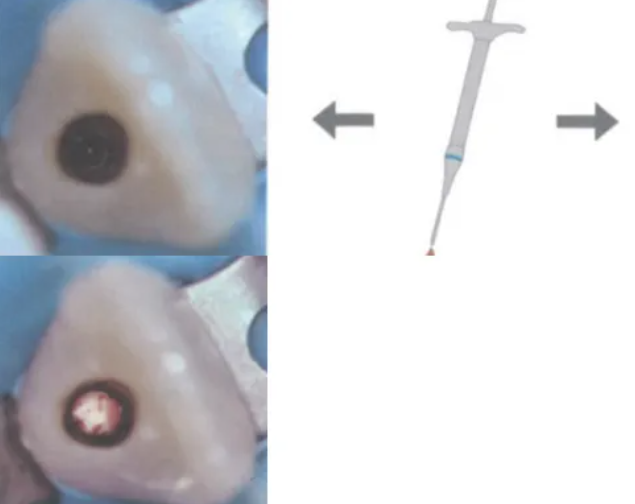
图3 牙髓再血管化治疗中,亲水性硅酸钙水门汀与血凝块(富含血细胞和纤维蛋白聚物不稳定)或胶原海绵支架材料接触(放置在血凝块上用于支撑亲水性硅酸钙水门汀),因此硅酸钙水门汀必须具有特殊的生物学和力学特性
为了改良MTA的以上缺点,一些新型亲水性硅酸钙水门汀的配方经过优化,不再使用诸如波特兰水门汀之类的天然材料,因为这些材料中可能含有影响治疗效果的微量元素或成分。取而代之的是合成材料,这些材料是由经过纯化并且满足临床要求的硅酸三钙制成的。这些新型硅酸钙水门汀与MTA具有相似的固化反应四,并且也能生成氢氧化钙(图4)。新型硅酸钙水门汀使用氧化锆或氧化钽来替代氧化铋,尽管这些替代材料具有较低的X线阻射性,但是降低了牙齿变色的风险。在硅酸钙水门汀的固化过程中,这些材料与氧化铋一样呈惰性状态,不会从材料中浸出。硅酸钙材料的液体成分中可能含有固化加速剂(例如氯化钙、水溶性聚合物),以便于临床操作,增强材料的机械特性。

图4 a为将亲水性硅酸钙水门汀浸泡在细胞培养液中,周化后使用扫描电镜观察其表面结构,可见硅酸钙水凝胶(CSH)沉积物、方解石结晶体、氢氧化钙和磷酸钙颗粒;b为人的牙髓干细胞黏附在硅酸三钙表面,并且伸展(箭头所示)
一些新型硅酸钙水门汀包含粉剂和液体,在使用前需要混合。市场上也出现了光固化硅酸钙水门汀,其操作简便、固化迅速并且可以调控。然而,这些都是树脂基材料,聚合反应会影响硅酸钙水门汀的固化以及氢氧化钙的释放。还必须注意的是,由于光固化硅酸钙水门汀中含有树脂单体,具有细胞毒性,而填料量导致其固化深度较浅会加剧这种情况,因此将严重损害其生物相容性。另外,填料颗粒的疏水性和含量将影响光固化硅酸钙水门汀固化反应所需液体的流通。目前磷酸钙、微硅粉等材料也被用作硅酸钙水门汀的添加剂;这些添加剂会影响氢氧化钙的形成,并且会影响生物相容性。
亲水性硅酸三钙与组织液的反应
亲水性硅酸三钙的一部分生物活性是由于这些材料能够与组织液相互作用并且在表面形成碳酸钙磷灰石。
在固化过程中,水解反应和离子交换导致副产物氢氧化钙的形成。碱性物质会促进硅酸钙颗粒表面形成无定形硅酸钙水凝胶,并且液体中的钙离子会被束缚。这些钙离子可在随后释放,并与含磷酸盐的液体中的磷酸氢盐发生反应。无定形磷酸钙在表面附近形成并沉淀在硅酸钙水凝胶中(图4)。这种磷酸钙会随着时间的推移而成熟,并形成碳酸钙磷灰石网。
由于碳酸钙磷灰石是矿化组织中典型的生物成分,因此在亲水性硅酸钙水门汀的细胞相容性和生物活性方面具有重要作用。血液中充满了钙和磷酸盐,因此在牙髓再血管化治疗过程中亲水性硅酸钙水门汀会与血凝块发生相互作用。
尽管体外研究已证实亲水性硅酸钙水门汀的生物活性(例如羟基磷灰石的形成)、抗菌活性和诱导矿化能力,但目前尚不清楚这些特性在体内是否发挥作用。几乎没有文献报道这些材料与血液或可吸收胶原海绵接触时发生的生物学行为。
然而,最近的研究表明,临床情况似乎与研究结果有所不同。有研究对牙髓再血管化失败病例中使用的波特兰水门汀进行分析,发现多孔材料表面富含碳酸钙而不是氢氧化钙或磷灰石。
亲水性硅酸钙的机械性能
尽管亲水性硅酸钙水门汀可以在潮湿环境中使用,但局部条件和污染会改变材料的固化特性并影响其机械性能在血清或组织液存在的情况下,亲水性硅酸钙水门汀的固化反应会受影响,同时显微硬度会降低。血液成分也会破坏亲水性硅酸钙水门汀的机械性能,使其抗压强度和显微硬度降低。研究发现,人工合成的硅酸三钙比MTA能更好地黏附在牙本质上,这是因为其颗粒较小,牙本质小管渗透更深。必须注意的是,氯己定、EDTA、抗生素糊剂等根管冲洗液或药物可能会使亲水性硅酸钙水门汀与牙本质的粘接强度降低,而次氯酸钠或生理盐水则没有影响,甚至氢氧化钙可以增强其黏附力。然而,目前亲水性硅酸钙水门汀的制造商并没有关于冲洗剂和药物的使用建议。在根尖屏障术中,亲水性硅酸钙水门汀与血管化的结缔组织接触,而在牙髓再血管化治疗中,亲水性硅酸钙水门汀与血凝块(富含血细胞和纤维蛋白凝聚物)或胶原海绵支架材料接触(图3)。尽管目前亲水性硅酸钙水门汀的配方经过改良后,已经成为首选的材料,但还是有必要研发出专门用于牙髓再血管化治疗的材料。
牙齿变色的原因
MTA的最初配方中包含氧化铋,这种显影剂会导致牙齿明显变色。由于接受牙髓再血管化治疗的牙齿通常是外伤后的前牙,因此牙齿的美观不容忽视。MTA在牙髓再血管化治疗中位于离冠部更近的位置(与根尖屏障术中不同),所以其周围变色的牙齿组织位于肉眼可见区域。亲水性硅酸钙水门汀导致牙齿变色取决于多种因素。为了降低牙齿变色的风险,新型亲水性硅酸钙水门汀的配方中使用氧化钽等物质来代替氧化铋。当MTA被血液污染时,血液成分被包裹在MTA的多孔结构中,可能导致变色。此外,血液成分与氧化铋发生反应也会导致牙本质着色。由于新型硅酸钙水门汀材料的均质性更高、孔隙更少,因此降低了接触血液后变色的风险。有研究发现,配方中不含氧化铋的硅酸钙水门汀在与次氯酸钠或氯己定等冲洗液接触后也会导致牙本质染色,但是程度较轻。因此,严格选择材料,例如使用不会导致牙齿变色的药物和不含氧化铋显影剂的亲水性硅酸钙水门汀,能够最大限度地降低牙齿变色的风险。

 梁静茹大方承认拔
梁静茹大方承认拔 刘涛烤瓷牙上热搜
刘涛烤瓷牙上热搜 十阿哥刘滨一口乱
十阿哥刘滨一口乱